화학1 산,염기 관련된 문제 질문드려요~
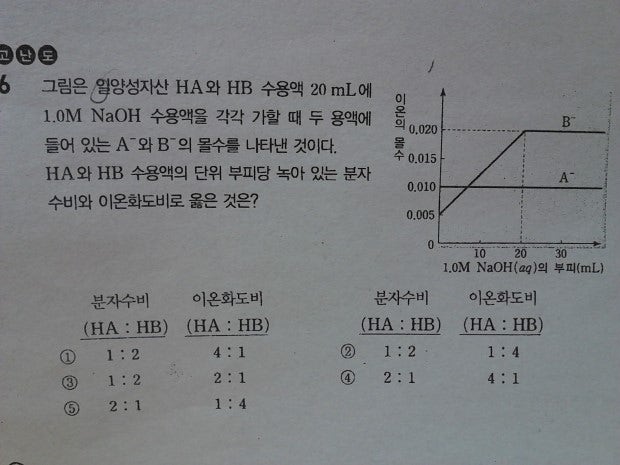


위에 문제 질문드려요~
1. B- 이온수가 NaOH의 넣어준 양과 무슨 관련이 있는거죠? 구경꾼이온은 반응에 참여 안하니까 넣어준 HB 20ml 안에 있는 B- 이온수는 변함이 없을것 같은데 증가하다가 일정하네요..
즉, 답지에선 A-이온이 강산의 짝염기이고, B-이온은 약산의 짝염기라서 위 모양의 그래프가 나왔다는데 강산 혹은 약산의 짝염기라는것과 NaOH를 넣어줌에 따라 A-, B-이온수의 변화와 무슨 관계가 있는지 궁금합니다~
2. 이온화도를 비교하는 부분에서, 이온화도= 이온화된 용질의 몰수/용질의 전체 몰수 아닌가요..?
근데 그래프 상에서 녹아있는 이온수와 전체 이온수에 대한 정보를 어디서 찾을수 있나요?;
0 XDK (+0)
유익한 글을 읽었다면 작성자에게 XDK를 선물하세요.
-
맛 들이면 안되는데 아
-
_참고서적: 『인간의 우주적 초라함과 삶의 부조리에 대하여』(최성호, 2019)...
-
새르비 2일차 0
오늘은 ㅇㅈ파티 안 하네. 일찍 자러 가야지. 일찍은 아닌가?
-
심심 8
저도 탈르비할까 고민 중..
-
인원체크 댓ㄱㄱ 16
이런 옯-창 쯧쯔 나레기
-
인증?? 2
주로 새벽에 인증 많이하시는 이유가 옯밍당하실까봐 그러시는거에요?
-
이 말을 해보고 싶었어요 ㅎ
-
재수를 경험해봐서 얼굴책에는 미안한 마음에 못 올리겠고 여기에라도 이렇게 남겨봐요...
-
조용조용 새르비 22
생존신고 뭐하시나영 다들
-
넘나 심심한 것.. 22
심심해오..
-
새르비 0
이시간까지 하는거 오랜만인데 낮타임보다 글이 많아 보이는건 착각인가요? 주말이라 그런가
-
우와 새르비 4
또 인증타임시작인가여 ㅋㅋㅋㅋ뀰잼
-
zara 15
zalza
-
작년 이맘때쯤에도 새르비 인증글들+펑펑글들을 보며 "우와 대단하다. 내년...
-
인증이 없었다고 한다... 나의 타이밍...못난 타이밍...
-
잠이 안온다 98
잠이안온다..
-
잠이안와 33
안와..잠와..잠안와..
-
제목이 곧 내용이지요.
-
음...대충 3번,4번으로 나눠쓸건데 필력이 장애라서 이해부탁드려요...
-
질문해보세요 61
뭘묻든 답은 할게요 다만 진실인지 거짓인지는 안알랴쥼
-
태그는 새르비와 9596..이지만수기 대신 질문 받는걸로...ㅎ 그리고 원래 늘...
-
지금 휴가 나온지 사흘째에 접어들고 잇네요 복귀...
-
박수칠때 떠나라 차승원 나왔던 영화제목이었는데 제목이 아이러니해서 되게...
-
뭐 수험생 생활 끝나고 새벽까지 안 자며 폰 들여다 보던그런 추억으로, 한 겨울...
-
강남 올때마다 놀랍니다ㅋㅋㅋㅋ여기가 한국이맞는지... 뉴스를 보면 살기는 힘들다는데...
-
1.여러분들은 언제부터 공부를 잘하기 시작하셨나요? 2.한 번쯤 엄청 추락해보신 적...
-
[새르비] 대화 글방! 33
댓글로 저와 대화 나눠요! 새르비 님들~제가 첫 질문으로님들은 어떤 계기로든 갑자기...
-
오늘은 새르비가 열릴 만큼 사람들이 있지 않나봐요? 지금은 인증 말고 대화...
-
ㅂㅂ... 17
너무 오래 있었네요...ㅠ ㅂㅂ..다들 긋잠 긋밤...ㅎ여기 있는 댓글은 최대한...
-
질문을 받아보죠 71
주제 상관 없습니당멘탈 관련 질문 재밌을듯그리고 저 남자 아닙니다 19살 여자입니다
-
M.orbi.kr 너무 답닺하시면 이쪽으로 들어가셔서 하세요 i.orbi...
-
서버 복구 후 60
글 리젠이 확실히 느림느림심심하네요 질문받아봤자... 맨날 하는 거고ㅋㅋㅋ재밌는 얘기 해주세요
-
장애인으로..
-
엽사인증ㅋㅋ 10
제대로된 사진이없어서 엽사로 승부!
-
안녕하십니까 어제 정말 올해 최초로 12시에 잠든 래인입니다덕분에 인증대란 놓침...
-
3시 25분까지 37
제가 오죽 심심했으면... 하나는 예전에 인증한거고 다른 하나는 고도의 뽀샵을 거친...
-
심심합니다 80
놀아주십시오
-
곧 2시 기념 50
잉여 질문 받아요 안잉여도 받습니다제가 잠들때까지 답함
-
저도 96인데 친구들 술마시러 가고 그러는데 저만 못가네요 ㅠㅠ 저같은분들 계신가요...
-
잘려고했는데 0
자려고만하면 인증글이 올라와서 못자겠다ㅠ
-
자러가야지 2
전단지알바때문에...ㅠㅠ
-
여자랑 말섞는게 너무 어색해요... 연애하고 싶은데 대화는 할수 있으련지...
-
이미 모 인강 사이트에서 인강을 찍는데어차피 제가 얼굴 가리고 하는건 아니니까요근데...
-
이런태그좋아 0
새르비굳
-
인증대란 2탄의 시작인건가요?
-
아이까지; 0
그들만이 아는 새르비의 이야기









































헐 이거 화학1으로 내려왔나요? ㄷㄷ
화학2 내용이었나요? ㅋㅋ;
어쩐지 어렵더라구요 ㅠㅠ
1. 네 이 부분이 밑에 말씀드린 중화적정과 더불어 가장 중요한, 심화 문제 풀이에 있어서 핵심적인 아이디어가 되는 부분입니다.
우선 B-이온은 구경꾼 이온이지만 다른 이온반응의 구경꾼 이온과 다르다는 사실을 매우 유념하여야 합니다
그 이유는 HB의 경우 '약산'입니다.
약산은 처음에 이온화가 대부분 되어있지 않습니다. 예를 들면 HB 1몰 있을때 H+ B-는 0.1몰 있다고 해보죠
여기서 H+가 들어온 OH-와 이온화가 됩니다
그러면 H+는 사라지죠 (B- 0.1몰은 그대로 있어요)
이때 다시 HB가 0.1몰 만큼 이온화가 됩니다
원래 있던 B-와, 새로 이온화된 B-가 합쳐져서 0.2몰로 양이 늘어나게 됩니다.
이런 과정이 중화점까지 쭉 이어지게 되있어요
그럼 HB가 약산인것을 어떻게 아느냐?
위의 아이디어를 이해하고 외워두면
위의 그래프처럼 B-의 이온이 증가하는 그래프를 보고 약산이라고 결론을 내릴수있어요
반드시 이해하고 암기하셔야할 사항입니다.
반면에 HA는 강산입니다
왜냐하면 만약에 약산이라면 위의 과정을 겪을테고, 아니니까 강산입니다
즉 처음부터 모든 HA가 이온화되어있습니다.
2. 말씀하신 부분 이온화도= 이온화된 용질의 몰수/용질의 전체 몰수 은 맞는내용입니다.
여기에서 이온화된 용질의 몰수와 용질의 전체 몰수는 사고를 통해서 찾아내야 합니다
처음의 이온화된 용질의 몰수가 0.010 mol / 0.005 mol 임은 바로 알수있습니다.
조금 헷갈릴수가 있어요. 막 이렇게 저렇게 복잡하게 생각할수있거든요.
아직은 중화가 전혀 되지 않은 상태이기 때문에, 위의 그래프의 몰수 (이온화된 몰수)를 통해서 비교를 할수가 있습니다.
그럼 그때 '용질의 전체 몰수'는 어떻게 알 수 있을까요?
nMV = n'M'V' 공식을 보셨을 겁니다. 그것을 사용하셔서 구하시면 됩니다
밑의 문제에서 말씀드렸듯이 약산이라고 해도 지속적으로 이온화가 일어나기 때문에
전체 몰수를 비교할때 약산/강산에 상관없이 위의 공식을 사용할수 있습니다.
그러면 B의 경우 중화점까지 넣어준 NaOH의 부피가 20mL입니다
그러므로 1 * 20 = 1 * 20 이므로 B의 농도 (이온화/이온화 안된걸 포함한 전체 용질의 농도)는 1M이 됩니다.
전체 용질의 몰수를 구해야 하므로 농도 x 부피 = 1 * 0.02 = 0.02 mol 입니다.
여기에서 A의 경우는 조금 다릅니다. 위의 그래프로는 중화점을 찾을수가 없어요
그러면 좀더 생각을 해봐야 합니다
A는 강산이므로 처음에 모든 용질이 이온화가 됩니다
그러므로 처음의 용질 몰수는 0.01 mol 입니다.
A의 이온화도 0.01/0.01 = 1 입니다 (강산이므로)
B의 이온화도 0.005/0.02 = 0.25 입니다
그러므로 이온화도의 비는 4 : 1 입니다.
이온화도 = 이온화된 용질의 몰수/ 용질의 전체 몰수 에서요~
분자의 이온화된 용질의 몰수는 맨처음 NaOH를 넣지 않은 상태에서의 몰수를 말하는 건가요?
그렇다면 이온화도를 구할때 B- 이온의 몰수가 맨 처음엔 0.005 였다가 중화점에서 0.02 이므로 0.005/0.02 이렇게 구해도 되는건가요?
네 결과적으로 보면 맞다고 해야 겠네요
B-이온이 중화점에 이르면 다 이온화가 되고,
H가 1가 산이므로 HB 한분자당 B-이온이 1개 나오므로 그렇게 구해도 됩니다.
2가 산일 경우에는 다르게 해야겠지요